Eine freie Initiative von Menschen bei mit online Lesekreisen, Übungsgruppen, Vorträgen ... |
| Use Google Translate for a raw translation of our pages into more than 100 languages. Please note that some mistranslations can occur due to machine translation. |
Chemische Reaktion: Unterschied zwischen den Versionen
imported>Odyssee Keine Bearbeitungszusammenfassung |
imported>Odyssee Keine Bearbeitungszusammenfassung |
||
| (22 dazwischenliegende Versionen desselben Benutzers werden nicht angezeigt) | |||
| Zeile 1: | Zeile 1: | ||
[[Datei:ThermiteFe2O3.JPG|mini|[[Wikipedia:Thermitreaktion|Thermitreaktion]] von [[Wikipedia:Eisen(III)-oxid]] und [[Aluminium]]]] | [[Datei:Natriumexplosion.jpg|mini|250px|Explosive Reaktion von [[Natrium]] und [[Wasser]]]] | ||
[[Datei:ThermiteFe2O3.JPG|mini|250px|[[Wikipedia:Thermitreaktion|Thermitreaktion]] von [[Wikipedia:Eisen(III)-oxid|Eisen(III)-oxid]] und [[Aluminium]]]] | |||
[[Datei:Triosephosphate isomerase.jpg|mini|250px|Bändermodell des Enzyms [[Wikipedia:Triosephosphatisomerase|Triosephosphatisomerase]] (TIM, TPI) nach {{PDB|2jk2}} ]] | |||
[[Datei:Energiediagramm-Enzymreaktion.svg|mini|250px||Energiediagramm der Enzym-Katalyse: Die Aktivierungsenergie (freie Aktivierungsenthalpie) wird im Vergleich zu unkatalysierten Reaktionen durch Stabilisierung des Übergangszustandes gesenkt. Die freie [[Wikipedia:Reaktionsenthalpie|Reaktionsenthalpie]] bleibt dabei unverändert.]] | |||
Eine '''chemische Reaktion''' ist ein [[Chemie|chemischer]] [[Prozess]], bei dem ein oder mehrere [[Chemisches Element|chemische Elemente]] oder [[chemische Verbindungen]] in andere chemische [[Stoff]]e umgewandelt werden. Dabei wird [[Energie]] z.B. in Form von [[Wärme]] und/oder [[Licht]] abgegeben oder verbraucht, die sog. ''' | Eine '''chemische Reaktion''' ist ein [[Chemie|chemischer]] [[Prozess]], bei dem ein oder mehrere [[Chemisches Element|chemische Elemente]] oder [[chemische Verbindungen]] in andere chemische [[Stoff]]e umgewandelt werden. Dabei wird „chemische“ [[Energie]] z.B. in Form von [[Wärme]] und/oder [[Licht]] abgegeben oder verbraucht, die sog. '''Reaktionsenthalpie''' ({{ELSalt|ἐν}} ''en'' „in“ und {{polytonisch|θάλπειν}} ''thálpein'' „erwärmen“): <math>\Delta H_\mathrm{R} = H_\mathrm{Produkte} - H_\mathrm{Edukte}</math>. So spricht man etwa auch von der '''Verbrennungsenthalpie''', der '''Bildungsenthalpie''', der '''Lösungsenthalpie''' usw. einer chemischen Verbindung. | ||
:<math>\Delta H_\mathrm{R} = H_\mathrm{Produkte} - H_\mathrm{Edukte}</math> | |||
== Aktivierungsenergie == | == Aktivierungsenergie == | ||
Damit eine Reaktion überhaupt in Gang kommt, ist die Zufuhr einer entsprechenden '''Aktivierungsenergie''' notwendig. So kann man etwa ein [[Wikipedia:Streichholz|Streichholz]] nur entzünden, wenn man ihm durch Reibung mechanische Energie bzw. Wärmeenergie zuführt. Bei scheinbar spontan ablaufenden Reaktionen wird die nötige [[Energie]] unmittelbar der Umgebungswärme entnommen. Je höher die zugeführte Wärme bzw. je geringer die benötigte Aktivierungsenergie ist, desto schneller läuft die Reaktion ab. Durch Beigabe kleiner Mengen eines spezifischen [[Katalysator]]s, der die nötige Aktivierungsenergie | Damit eine Reaktion überhaupt in Gang kommt, ist die Zufuhr einer entsprechenden '''Aktivierungsenergie''' notwendig. So kann man etwa ein [[Wikipedia:Streichholz|Streichholz]] nur entzünden, wenn man ihm durch Reibung mechanische Energie bzw. Wärmeenergie zuführt. Bei scheinbar spontan ablaufenden Reaktionen wird die nötige [[Energie]] unmittelbar der Umgebungswärme entnommen. Je höher die zugeführte Wärme bzw. je geringer die benötigte Aktivierungsenergie ist, desto schneller läuft die Reaktion ab. Durch Beigabe kleiner Mengen eines spezifischen [[Katalysator]]s, der die nötige Aktivierungsenergie verringert, kann die Reaktion gegebenenfalls wesentlich beschleunigt werden. | ||
== Beispiele == | == Beispiele == | ||
Eine einfache chemische Reaktion ist beispielsweise die [[Verbrennung]], bei der ein brennbarer Stoff mit dem [[Sauerstoff]] ([[lat.]] ''Oxygenium''; abgeleitet von {{ELSalt|ὀξύς}} ''oxys'' „scharf, spitz, sauer“ und {{polytonisch|γεν-}} ''gen-'' „erzeugen“) der [[Luft]] unter Energieabgabe reagiert. So entsteht etwa bei der Verbrennung von [[Kohlenstoff]] mit einer ausreichenden Menge Sauerstoff das gasförmige [[Wikipedia:Kohlendioxid|Kohlendioxid]] (bzw. bei Sauerstoffmangel das sehr giftige [[Wikipedia:Kohlenmonoxid|Kohlenmonoxid]]): | Eine einfache chemische Reaktion ist beispielsweise die [[Verbrennung]], bei der ein brennbarer Stoff mit dem [[Sauerstoff]] ([[lat.]] ''Oxygenium''; abgeleitet von {{ELSalt|ὀξύς}} ''oxys'' „scharf, spitz, sauer“ und {{polytonisch|γεν-}} ''gen-'' „erzeugen“) der [[Luft]] unter Energieabgabe reagiert. So entsteht etwa bei der Verbrennung von [[Kohlenstoff]] mit einer ausreichenden Menge Sauerstoff das gasförmige [[Wikipedia:Kohlendioxid|Kohlendioxid]] (bzw. bei Sauerstoffmangel das sehr giftige [[Wikipedia:Kohlenmonoxid|Kohlenmonoxid]]): | ||
:<math>\mathrm{C\ +\ O_2 \longrightarrow \ CO_2 \ ; \quad \Delta} H = -394 \; \mathrm{kJ/mol}</math><ref> | :<math>\mathrm{C\ +\ O_2 \longrightarrow \ CO_2 \ ; \quad \Delta} H = -394 \; \mathrm{kJ/mol}</math><ref>''Schülerduden Chemie'', Bibliografisches Institut & F.A. Brockhaus AG, Mannheim 2007, ISBN 978-3-411-05386-5, S. 195.</ref> | ||
Eine anderes Beispiel ist die rechts im Bild gezeigte stark exotherme [[Wikipedia:Thermitreaktion|Thermitreaktion]] von [[Wikipedia:Eisen(III)-oxid|Eisen(III)-oxid]] und [[Aluminium]], bei der Temperaturen bis über 2000 °C erreicht werden: | |||
:<math>\mathrm{Fe_2O_3 + 2 \ Al \longrightarrow Al_2O_3 + 2 \ Fe; \quad \Delta} H = -851{,}5 \; \mathrm{kJ/mol}</math> | |||
Das Bild rechts oben zeigt die Reaktion von metallischem [[Natrium]] mit [[Wasser]]. Das bei der Reaktion gebildete [[Wasserstoff]]gas entzündet sich, verbrennt explosionsartig und reißt geschmolzene Natriumtröpfchen mit, die zu [[Wikipedia:Natriumoxid|Natriumoxid]] bzw. [[Wikipedia:Natriumperoxid|Natriumperoxid]] verbrennen: | |||
:<math>\mathrm{2 \ Na + 2 \ H_2O \rightarrow 2 \ NaOH + H_2}; </math> | |||
:<math>\mathrm{4\ Na + O_2 \longrightarrow 2\ Na_2O;} {\quad \Delta} H = -431{,}6 \; \mathrm{kJ/mol}</math> | |||
:<math>\mathrm{2\ Na_2O + O_2 \longrightarrow 2\ Na_2O_2;} {\quad \Delta} H = -79{,}6 \; \mathrm{kJ/mol}</math> | |||
=== Friedrich Wöhlers Harnstoffsynthese (1828) === | |||
Als es dem [[Wikipedia:Deutschland|deutschen]] [[Chemiker]] [[Wikipedia:Friedrich Wöhler|Friedrich Wöhler]] (1800-1882) erstmals [[Wikipedia:1828|1828]] gelang, [[Harnstoff]] aus der salzartigen [[Anorganische Verbindung|anorganischen Verbindung]] [[Wikipedia:Ammoniumcyanat|Ammoniumcyanat]] herzustellen, galt dies als Beweis, dass die Synthese organischer Verbindungen keiner besonderen „[[Lebenskraft]]“ bedürfe: | |||
:<math>\mathrm{AgNCO + NH_4Cl \rightarrow NH_4(NCO) + AgCl}</math> | |||
Wöhler erkannte dabei ganz richtig, dass die intermediär gebildete Verbindung [[Wikipedia:Ammoniumcyanat|Ammoniumcyanat]] (NH<sub>4</sub>NCO) die eigentliche Harnstoffquelle darstellte: | |||
: [[Datei:Urea Synthesis Woehler.png|ohne|300px|Harnstoffsynthese nach Wöhler]] | |||
=== Biochemische Reaktionen === | |||
[[Biochemie|Biochemische]] Prozesse, die für den [[Stoffwechsel]] aller [[Lebewesen]] von zentraler Bedeutung sind, laufen stets nur in Anwesenheit eines meist sehr komplex gebauten Katalysators in nennenswerter Geschwindigkeit ab. So katalysiert etwa das Enzym [[Wikipedia:Triosephosphatisomerase|Triosephosphatisomerase]] (TIM, TPI) in einem Teilschritt der [[Wikipedia:Glycolyse|Glycolyse]], dem lebenswichtigen [[Zucker]]abbau in allen [[Organismen]], die Umwandlung von [[Wikipedia:Dihydroxyacetonphosphat|Dihydroxyacetonphosphat]] (DHAP) zu [[Wikipedia:Glycerinaldehyd-3-phosphat|Glycerinaldehyd-3-phosphat]] (GAP): | |||
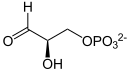
:<math>\ | [[Datei:Dihydroxyacetonphosphat Skelett.svg|140px]] <math>\rightleftharpoons</math> [[Datei:D-Glycerinaldehyd-3-phosphat Skelett.svg|130px]] | ||
== Siehe auch == | == Siehe auch == | ||
Version vom 15. April 2018, 23:01 Uhr




Eine chemische Reaktion ist ein chemischer Prozess, bei dem ein oder mehrere chemische Elemente oder chemische Verbindungen in andere chemische Stoffe umgewandelt werden. Dabei wird „chemische“ Energie z.B. in Form von Wärme und/oder Licht abgegeben oder verbraucht, die sog. Reaktionsenthalpie (griech. ἐν en „in“ und θάλπειν thálpein „erwärmen“): . So spricht man etwa auch von der Verbrennungsenthalpie, der Bildungsenthalpie, der Lösungsenthalpie usw. einer chemischen Verbindung.
Aktivierungsenergie
Damit eine Reaktion überhaupt in Gang kommt, ist die Zufuhr einer entsprechenden Aktivierungsenergie notwendig. So kann man etwa ein Streichholz nur entzünden, wenn man ihm durch Reibung mechanische Energie bzw. Wärmeenergie zuführt. Bei scheinbar spontan ablaufenden Reaktionen wird die nötige Energie unmittelbar der Umgebungswärme entnommen. Je höher die zugeführte Wärme bzw. je geringer die benötigte Aktivierungsenergie ist, desto schneller läuft die Reaktion ab. Durch Beigabe kleiner Mengen eines spezifischen Katalysators, der die nötige Aktivierungsenergie verringert, kann die Reaktion gegebenenfalls wesentlich beschleunigt werden.
Beispiele
Eine einfache chemische Reaktion ist beispielsweise die Verbrennung, bei der ein brennbarer Stoff mit dem Sauerstoff (lat. Oxygenium; abgeleitet von griech. ὀξύς oxys „scharf, spitz, sauer“ und γεν- gen- „erzeugen“) der Luft unter Energieabgabe reagiert. So entsteht etwa bei der Verbrennung von Kohlenstoff mit einer ausreichenden Menge Sauerstoff das gasförmige Kohlendioxid (bzw. bei Sauerstoffmangel das sehr giftige Kohlenmonoxid):
Eine anderes Beispiel ist die rechts im Bild gezeigte stark exotherme Thermitreaktion von Eisen(III)-oxid und Aluminium, bei der Temperaturen bis über 2000 °C erreicht werden:
Das Bild rechts oben zeigt die Reaktion von metallischem Natrium mit Wasser. Das bei der Reaktion gebildete Wasserstoffgas entzündet sich, verbrennt explosionsartig und reißt geschmolzene Natriumtröpfchen mit, die zu Natriumoxid bzw. Natriumperoxid verbrennen:
Friedrich Wöhlers Harnstoffsynthese (1828)
Als es dem deutschen Chemiker Friedrich Wöhler (1800-1882) erstmals 1828 gelang, Harnstoff aus der salzartigen anorganischen Verbindung Ammoniumcyanat herzustellen, galt dies als Beweis, dass die Synthese organischer Verbindungen keiner besonderen „Lebenskraft“ bedürfe:
Wöhler erkannte dabei ganz richtig, dass die intermediär gebildete Verbindung Ammoniumcyanat (NH4NCO) die eigentliche Harnstoffquelle darstellte:
Biochemische Reaktionen
Biochemische Prozesse, die für den Stoffwechsel aller Lebewesen von zentraler Bedeutung sind, laufen stets nur in Anwesenheit eines meist sehr komplex gebauten Katalysators in nennenswerter Geschwindigkeit ab. So katalysiert etwa das Enzym Triosephosphatisomerase (TIM, TPI) in einem Teilschritt der Glycolyse, dem lebenswichtigen Zuckerabbau in allen Organismen, die Umwandlung von Dihydroxyacetonphosphat (DHAP) zu Glycerinaldehyd-3-phosphat (GAP):
Siehe auch
- Chemische Reaktion - Artikel in der deutschen Wikipedia
- Aktivierungsenergie - Artikel in der deutschen Wikipedia
- Reaktionsenthalpie - Artikel in der deutschen Wikipedia
Einzelnachweise
- ↑ Schülerduden Chemie, Bibliografisches Institut & F.A. Brockhaus AG, Mannheim 2007, ISBN 978-3-411-05386-5, S. 195.