Eine freie Initiative von Menschen bei mit online Lesekreisen, Übungsgruppen, Vorträgen ... |
| Use Google Translate for a raw translation of our pages into more than 100 languages. Please note that some mistranslations can occur due to machine translation. |
Anonymität und Chemische Reaktion: Unterschied zwischen den Seiten
imported>Odyssee |
imported>Odyssee |
||
| Zeile 1: | Zeile 1: | ||
'' | [[Datei:Natriumexplosion.jpg|mini|250px|Explosive Reaktion von [[Natrium]] und [[Wasser]]]] | ||
[[Datei:AktivierungsenergieV2.svg|miniatur|250px|Die Beziehung zwischen Aktivierungsenergie ({{polytonisch|''E<sub>a</sub>''}}) und [[Bildungsenthalpie]] ({{polytonisch|Δ''H''}}) bei einer exothermen Reaktion. Dabei muss der durch den energiereichen Übergangszustand bedingte Energieberg überwunden werden. Durch einen Katalysator bildet sich ein Übergangszustand mit geringerer Energie, wodurch die Reaktionsgeschwindigkeit erhöht wird.]] | |||
[[Datei:ThermiteFe2O3.JPG|mini|250px|[[Wikipedia:Thermitreaktion|Thermitreaktion]] von [[Wikipedia:Eisen(III)-oxid|Eisen(III)-oxid]] und [[Aluminium]]]] | |||
[[Datei:Triosephosphate isomerase.jpg|mini|250px|Bändermodell des Enzyms [[Wikipedia:Triosephosphatisomerase|Triosephosphatisomerase]] (TIM, TPI) nach {{PDB|2jk2}} ]] | |||
[[Datei:Energiediagramm-Enzymreaktion.svg|mini|250px||Energiediagramm der Enzym-Katalyse: Die Aktivierungsenergie (freie Aktivierungsenthalpie) wird im Vergleich zu unkatalysierten Reaktionen durch Stabilisierung des Übergangszustandes gesenkt. Die freie [[Wikipedia:Reaktionsenthalpie|Reaktionsenthalpie]] bleibt dabei unverändert.]] | |||
Eine '''chemische Reaktion''' ist ein [[Chemie|chemischer]] [[Prozess]], bei dem ein oder mehrere [[Chemisches Element|chemische Elemente]] oder [[chemische Verbindungen]] als '''Reaktanten''' (seltener '''Reaktanden''' oder veraltet '''Edukte''', von [[lat.]] ''eductum'' „Herausgeführtes“) in andere chemische [[Stoff]]e, die '''Produkte''', umgewandelt werden. Sind diese ebenfalls reaktionsfreudig, so kann es zu weiteren '''Folgereaktionen''' kommen. Viele Reaktionen führen erst über ein oder mehrere '''Zwischenprodukte''' ('''Intermediate''') zum [[Endprodukt]], das isoliert und gereinigt wird. | |||
== | == Exotherme und endotherme Reaktionen == | ||
Bei chemischen Reaktionen wird „chemische“ [[Energie]] z.B. in Form von [[Wärme]] und/oder [[Licht]] abgegeben oder verbraucht, die sog. '''Reaktionsenthalpie''' (von {{ELSalt|ἐν}} ''en'' „in“ und {{polytonisch|θάλπειν}} ''thálpein'' „erwärmen“) oder '''Reaktionswärme''': <math>\Delta H_\mathrm{R} = H_\mathrm{Produkte} - H_\mathrm{Edukte}</math>. Eine '''exotherme Reaktion''', beispielsweise eine [[Verbrennung (Chemie)|Verbrennung]], setzt Energie frei ( <math>\Delta H_\mathrm{R} < 0</math> ), eine '''endothermen Reaktion''' hingegen verbraucht Energie ( <math>\Delta H_\mathrm{R} > 0</math> ). | |||
Nach dem zuerst 1851 von dem dänischen Chemiker [[w:Julius Thomsen|Julius Thomsen]] (1826-1909) und 1866 auch von dem französischen Chemiker [[w:Marcelin Berthelot|Marcelin Berthelot]] (1827-1907) aufgestellten und nach ihnen benannten '''Thomsen-Berthelotschen Prinzip''' dachte man zunächst fälschlich, dass die Reaktionswärme ein geeignetes Maß für die [[Affinität (Chemie)|Triebkraft]] einer chemischen Reaktion sei<ref>Otto Sackur, Cl. v. Simson: ''Lehrbuch der Thermochemie und Thermodynamik'', Verlag von Julius Springer, Berlin 1928, S. 94f. [https://books.google.at/books?id=nxmhBgAAQBAJ&pg=PA94 google]</ref>. Entscheidend ist aber vielmehr die nachstehend beschriebene [[freie Enthalpie]].<ref>{{Holleman-Wiberg| Auflage=71 |Startseite=57 |Endseite=58}}</ref> Das Thomsen-Berthelotsche Prinzip ist nur bei tiefen Temperaturen näherungsweise gültig, weil dann der [[Entropie]]-Term der freien Enthalpie klein genug ist, um vernachlässigt zu werden. | |||
== Exergone und endergone Reaktionen == | |||
Für den Ablauf einer chemischen Reaktion ist die Änderung der [[freie Enthalpie|freien Enthalpie]] <math>\Delta G</math> (auch [[Gibbs-Energie]] genannt) maßgeblich. Sie berücksichtigt auch die Änderung der [[Entropie]] <math>\Delta S</math>. Mit der [[Absolute Temperatur|absoluten Temperatur]] <math>T</math> ergibt sich für die '''freie Reaktionsenthalpie''' folgender Zusammenhang: | |||
:<math>\Delta G = \Delta H - T \cdot \Delta S </math> | |||
Für '''exergone Reaktionen''' ist <math>\Delta G < 0</math>; sie laufen als '''spontane Reaktion''' in Richtung der [[Produkt (Chemie)|Produkte]] ab. Bei '''endergonen Reaktionen''' mit <math>\Delta G > 0</math> ist die Rückreaktion begünstigt und bei <math>\Delta G = 0</math> stehen Hin- und Rückreaktion im Gleichgewicht. Mithilfe der freien Enthalpie und der [[Universelle Gaskonstante|universellen Gaskonstante]] <math>R</math> lässt sich entsprechend die Gleichgewichtskonstante <math>K</math> der Reaktion berechnen: | |||
im | |||
== | :<math>K = \exp \left( \frac{-\Delta G}{R \cdot T} \right) </math> | ||
== Aktivierungsenergie == | |||
Damit eine Reaktion, egal ob exotherm oder endotherm, überhaupt in Gang kommt, ist die Zufuhr einer entsprechenden '''Aktivierungsenergie''' <math>E_\mathrm{A}</math> notwendig, die üblicherweise in [[Joule]] pro [[mol]] (J·mol<sup>−1</sup>) angegeben wird. So kann man etwa ein [[Wikipedia:Streichholz|Streichholz]] nur entzünden, wenn man ihm durch Reibung mechanische Energie bzw. Wärmeenergie zuführt. Bei scheinbar spontan ablaufenden Reaktionen wird die nötige [[Energie]] unmittelbar der Umgebungswärme entnommen. Je höher die zugeführte Wärme bzw. je geringer die benötigte Aktivierungsenergie ist, desto schneller läuft die Reaktion ab. Nach der [[1884]] von dem niederländischen Chemiker [[w:Jacobus Henricus van ’t Hoff|Jacobus Henricus van ’t Hoff]] aufgestellten '''RGT-Regel''' ('''R'''eaktions'''g'''eschwindigkeit-'''T'''emperatur-Regel, auch '''van-’t-Hoff’sche Regel''') gilt, dass eine Temperaturerhöhung um 10 [[Kelvin|K]] die [[Reaktionsgeschwindigkeit]] ungefähr verdoppelt. Durch Beigabe kleiner Mengen eines spezifischen [[Katalysator]]s, der die nötige Aktivierungsenergie verringert, kann die Reaktion gegebenenfalls wesentlich beschleunigt werden. | |||
Die Temperaturabhängigkeit der [[Geschwindigkeitskonstante]]n <math>k</math> einer chemischen Reaktion kann durch die von [[w:Svante Arrhenius|Svante Arrhenius]] empirisch aufgestellte und später nach ihm benannte '''Arrhenius-Gleichung''' ermittelt werden: | |||
{{Notiz|<math>k = A \cdot \mathrm{e}^{-\frac{E_\mathrm{A}}{R \cdot T}}</math> '''Arrhenius-Gleichung'''}} | |||
dabei ist | |||
:<math>A</math> ein präexponentieller Faktor, der in vielen Fällen als ''nicht'' temperaturabhängig angenommen werden kann, | |||
:<math>E_\mathrm{A}</math> die Aktivierungsenergie in [[Joule|J]]/[[mol]], | |||
:<math>R = 8{,}314 \mathrm{J/K\,mol}</math> die [[universelle Gaskonstante]], | |||
:<math>T</math> die [[absolute Temperatur]] in [[Kelvin|K]]. | |||
Der hier auf ein [[Mol]] bezogene '''Boltzmann-Faktor''' <math>\mathrm{e}^{-\frac{E_\mathrm{A}}{R \cdot T}}</math> gibt dabei an, wie viele Teilchen pro Mol im statistischen Durchschnitt die nötige Aktivierungsenergie <math>E_\mathrm{A}</math> bei der gegebenen [[Thermische Energie|thermischen Energie]] <math>R \cdot T</math> aufbringen können. | |||
== Reaktionsgleichung == | |||
Eine '''Reaktionsgleichung''' beschreibt eine chemische Reaktion symbolisch im [[stöchiometrisch]] richtigen Verhältnis. Auf der linken Seite der Gleichung stehen die Reaktanten, versehen mit einer entsprechenden '''stöchiometrischen Zahl''' <math>\nu</math><ref>{{Gold Book|stoichiometric number|S06025|Version=2.3.1}}</ref> (auch '''stöchiometrischer Koeffizient''', '''Stöchiometriezahl''' oder '''Stöchiometriefaktor''' genannt). Dann folgt ein Reaktionspfeil (<math>\rightarrow</math>) bzw. bei einer Gleichgewichtsreaktion ein Doppelpfeil (<math>\rightleftharpoons</math>), und auf der rechten Seite stehen die Produkte. Gegebenenfall wird gesondert auch die Reaktionsenthalpie angegeben. Für die Knallgasreaktion, bei der '''g'''asförmiger Wasserstoff <math>\mathrm {H_{2(g)}}</math> mit '''g'''asförmigem Sauerstoff <math>\mathrm {O_{2(g)}}</math> explosionsartig zu '''l'''iquidem (=flüssigen) Wasser <math>\mathrm {H_2O_{(l)}}</math> reagiert, ergibt sich beispielsweise unter Berücksichtigung der [[Aggregatzustand|Aggregatzustände]] folgende Schreibweise: | |||
:<math>\mathrm{2 \ H_{2(g)} + O_{2(g)} \longrightarrow 2 \ H_2O_{(l)} \ ;} \ \Delta H = -572 \, \mathrm{kJ/mol}</math> | |||
=== Reaktionsschema === | |||
Der prinzipielle Ablauf einer chemischen Reaktion kann auch durch ein '''Reaktionsschema''' veranschaulicht werden, bei dem die stöchiometrischen Verhältnisse unberücksichtigt bleiben. Das kann z.B. in Form einer allgemein verständlichen Wortgleichung geschehen, z.B. für die Knallgasreaktion: | |||
:<math>\mathrm {Wasserstoff + Sauerstoff \longrightarrow Wasser}</math> | |||
In der [[Organische Chemie|organischen Chemie]] werden im Reaktionsschema zumeist nur die [[Strukturformel]]n der beteiligten [[Organische Verbindung|organischen Verbindungen]] angeschrieben. So ergibt sich etwa für die [[säure]]katalysierte Abspaltung von Wasser aus [[w:2-Pentanol|2-Pentanol]] folgendes Schema: | |||
[[Datei:Saytzeffdehydrogenisierung von 2 pentanol.svg|center|600px|Dehydratisierung von 2-Penanol zu einem Gemisch von drei isomeren Pentenen.]] | |||
Als Nebenprodukt entsteht [[w:Pentene|1-Penten]] (links direkt nach dem Reaktionspfeil) und als Hauptprodukte die beiden [[Isomere]] [[w:Pentene|(''E'')-2-Penten]] (Mitte) und [[w:Pentene|(''Z'')-2-Penten]] (rechts); die Säurekatalyse und das abgepaltene Wasser werden als bekannt vorausgesetzt und nicht angeschrieben. | |||
== Beispiele == | |||
Eine einfache chemische Reaktion ist die [[Verbrennung]], bei der ein brennbarer Stoff mit dem [[Sauerstoff]] ([[lat.]] ''Oxygenium''; abgeleitet von {{ELSalt|ὀξύς}} ''oxys'' „scharf, spitz, sauer“ und {{polytonisch|γεν-}} ''gen-'' „erzeugen“) der [[Luft]] unter Energieabgabe reagiert. So entsteht etwa bei der Verbrennung von [[Kohlenstoff]] mit einer ausreichenden Menge Sauerstoff das gasförmige [[Wikipedia:Kohlendioxid|Kohlendioxid]] (bzw. bei Sauerstoffmangel das sehr giftige [[Wikipedia:Kohlenmonoxid|Kohlenmonoxid]]): | |||
:<math>\mathrm{C\ +\ O_2 \longrightarrow \ CO_2 \ ; \quad \Delta} H = -394 \; \mathrm{kJ/mol}</math><ref>''Schülerduden Chemie'', Bibliografisches Institut & F.A. Brockhaus AG, Mannheim 2007, ISBN 978-3-411-05386-5, S. 195.</ref> | |||
Eine anderes Beispiel ist die rechts im Bild gezeigte stark exotherme [[Wikipedia:Thermitreaktion|Thermitreaktion]] von [[Wikipedia:Eisen(III)-oxid|Eisen(III)-oxid]] und [[Aluminium]], bei der Temperaturen bis über 2000 °C erreicht werden: | |||
:<math>\mathrm{Fe_2O_3 + 2 \ Al \longrightarrow Al_2O_3 + 2 \ Fe; \quad \Delta} H = -851{,}5 \; \mathrm{kJ/mol}</math> | |||
Das Bild rechts ganz oben zeigt die Reaktion von metallischem [[Natrium]] mit [[Wasser]]. Das bei der Reaktion gebildete [[Wasserstoff]]gas entzündet sich, verbrennt explosionsartig und reißt geschmolzene Natriumtröpfchen mit, die zu [[Wikipedia:Natriumoxid|Natriumoxid]] bzw. [[Wikipedia:Natriumperoxid|Natriumperoxid]] verbrennen: | |||
:<math>\mathrm{2 \ Na + 2 \ H_2O \rightarrow 2 \ NaOH + H_2}; </math> | |||
:<math>\mathrm{4\ Na + O_2 \rightarrow 2\ Na_2O;} {\quad \Delta} H = -431{,}6 \; \mathrm{kJ/mol}</math> | |||
:<math>\mathrm{2\ Na_2O + O_2 \rightarrow 2\ Na_2O_2;} {\quad \Delta} H = -79{,}6 \; \mathrm{kJ/mol}</math> | |||
=== Friedrich Wöhlers Harnstoffsynthese (1828) === | |||
Als es dem [[Deutschland|deutschen]] [[Chemiker]] [[Friedrich Wöhler]] (1800-1882) erstmals [[1828]] gelang, [[Harnstoff]] aus der salzartigen [[Anorganische Verbindung|anorganischen Verbindung]] [[Ammoniumcyanat]] herzustellen, galt dies als Beweis, dass die Synthese organischer Verbindungen keiner besonderen „[[Lebenskraft]]“ bedürfe: | |||
:<math>\mathrm{AgNCO + NH_4Cl \rightarrow NH_4(NCO) + AgCl}</math> | |||
Wöhler erkannte dabei ganz richtig, dass die intermediär gebildete Verbindung [[Ammoniumcyanat]] (NH<sub>4</sub>NCO) die eigentliche Harnstoffquelle darstellte: | |||
: [[Datei:Urea Synthesis Woehler.png|ohne|300px|Harnstoffsynthese nach Wöhler]] | |||
=== Biochemische Reaktionen === | |||
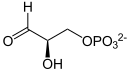
[[Biochemie|Biochemische]] Prozesse, die für den [[Stoffwechsel]] aller [[Lebewesen]] von zentraler Bedeutung sind, laufen stets nur in Anwesenheit eines meist sehr komplex gebauten Katalysators in nennenswerter Geschwindigkeit ab. So katalysiert etwa das Enzym [[Wikipedia:Triosephosphatisomerase|Triosephosphatisomerase]] (TIM, TPI) in einem Teilschritt der [[Wikipedia:Glycolyse|Glycolyse]], dem lebenswichtigen [[Zucker]]abbau in allen [[Organismen]], die Umwandlung von [[Wikipedia:Dihydroxyacetonphosphat|Dihydroxyacetonphosphat]] (DHAP) zu [[Wikipedia:Glycerinaldehyd-3-phosphat|Glycerinaldehyd-3-phosphat]] (GAP): | |||
[[Datei:Dihydroxyacetonphosphat Skelett.svg|140px]] <math>\rightleftharpoons</math> [[Datei:D-Glycerinaldehyd-3-phosphat Skelett.svg|130px]] | |||
=== Photochemische Reaktion === | |||
'''Photochemische Reaktionen''' werden nicht primär durch [[Wärme]], sondern durch [[Licht]]energie bewirkt bzw. ausgelöst. Ein komplexes Beispiel dafür ist die [[Photosynthese]]. | |||
== Siehe auch == | |||
* {{WikipediaDE|Kategorie:Chemische Reaktion}} | |||
* {{WikipediaDE|Chemische Reaktion}} | |||
* {{WikipediaDE|Aktivierungsenergie}} | |||
* {{WikipediaDE|Reaktionsenthalpie}} | |||
== Einzelnachweise == | |||
<references /> | |||
[[Kategorie: | [[Kategorie:Chemische Reaktion|!]] | ||
Version vom 15. August 2019, 18:56 Uhr





Eine chemische Reaktion ist ein chemischer Prozess, bei dem ein oder mehrere chemische Elemente oder chemische Verbindungen als Reaktanten (seltener Reaktanden oder veraltet Edukte, von lat. eductum „Herausgeführtes“) in andere chemische Stoffe, die Produkte, umgewandelt werden. Sind diese ebenfalls reaktionsfreudig, so kann es zu weiteren Folgereaktionen kommen. Viele Reaktionen führen erst über ein oder mehrere Zwischenprodukte (Intermediate) zum Endprodukt, das isoliert und gereinigt wird.
Exotherme und endotherme Reaktionen
Bei chemischen Reaktionen wird „chemische“ Energie z.B. in Form von Wärme und/oder Licht abgegeben oder verbraucht, die sog. Reaktionsenthalpie (von griech. ἐν en „in“ und θάλπειν thálpein „erwärmen“) oder Reaktionswärme: . Eine exotherme Reaktion, beispielsweise eine Verbrennung, setzt Energie frei ( ), eine endothermen Reaktion hingegen verbraucht Energie ( ).
Nach dem zuerst 1851 von dem dänischen Chemiker Julius Thomsen (1826-1909) und 1866 auch von dem französischen Chemiker Marcelin Berthelot (1827-1907) aufgestellten und nach ihnen benannten Thomsen-Berthelotschen Prinzip dachte man zunächst fälschlich, dass die Reaktionswärme ein geeignetes Maß für die Triebkraft einer chemischen Reaktion sei[1]. Entscheidend ist aber vielmehr die nachstehend beschriebene freie Enthalpie.[2] Das Thomsen-Berthelotsche Prinzip ist nur bei tiefen Temperaturen näherungsweise gültig, weil dann der Entropie-Term der freien Enthalpie klein genug ist, um vernachlässigt zu werden.
Exergone und endergone Reaktionen
Für den Ablauf einer chemischen Reaktion ist die Änderung der freien Enthalpie (auch Gibbs-Energie genannt) maßgeblich. Sie berücksichtigt auch die Änderung der Entropie . Mit der absoluten Temperatur ergibt sich für die freie Reaktionsenthalpie folgender Zusammenhang:
Für exergone Reaktionen ist ; sie laufen als spontane Reaktion in Richtung der Produkte ab. Bei endergonen Reaktionen mit ist die Rückreaktion begünstigt und bei stehen Hin- und Rückreaktion im Gleichgewicht. Mithilfe der freien Enthalpie und der universellen Gaskonstante lässt sich entsprechend die Gleichgewichtskonstante der Reaktion berechnen:
Aktivierungsenergie
Damit eine Reaktion, egal ob exotherm oder endotherm, überhaupt in Gang kommt, ist die Zufuhr einer entsprechenden Aktivierungsenergie notwendig, die üblicherweise in Joule pro mol (J·mol−1) angegeben wird. So kann man etwa ein Streichholz nur entzünden, wenn man ihm durch Reibung mechanische Energie bzw. Wärmeenergie zuführt. Bei scheinbar spontan ablaufenden Reaktionen wird die nötige Energie unmittelbar der Umgebungswärme entnommen. Je höher die zugeführte Wärme bzw. je geringer die benötigte Aktivierungsenergie ist, desto schneller läuft die Reaktion ab. Nach der 1884 von dem niederländischen Chemiker Jacobus Henricus van ’t Hoff aufgestellten RGT-Regel (Reaktionsgeschwindigkeit-Temperatur-Regel, auch van-’t-Hoff’sche Regel) gilt, dass eine Temperaturerhöhung um 10 K die Reaktionsgeschwindigkeit ungefähr verdoppelt. Durch Beigabe kleiner Mengen eines spezifischen Katalysators, der die nötige Aktivierungsenergie verringert, kann die Reaktion gegebenenfalls wesentlich beschleunigt werden.
Die Temperaturabhängigkeit der Geschwindigkeitskonstanten einer chemischen Reaktion kann durch die von Svante Arrhenius empirisch aufgestellte und später nach ihm benannte Arrhenius-Gleichung ermittelt werden:
| Arrhenius-Gleichung |
dabei ist
- ein präexponentieller Faktor, der in vielen Fällen als nicht temperaturabhängig angenommen werden kann,
- die Aktivierungsenergie in J/mol,
- die universelle Gaskonstante,
- die absolute Temperatur in K.
Der hier auf ein Mol bezogene Boltzmann-Faktor gibt dabei an, wie viele Teilchen pro Mol im statistischen Durchschnitt die nötige Aktivierungsenergie bei der gegebenen thermischen Energie aufbringen können.
Reaktionsgleichung
Eine Reaktionsgleichung beschreibt eine chemische Reaktion symbolisch im stöchiometrisch richtigen Verhältnis. Auf der linken Seite der Gleichung stehen die Reaktanten, versehen mit einer entsprechenden stöchiometrischen Zahl [3] (auch stöchiometrischer Koeffizient, Stöchiometriezahl oder Stöchiometriefaktor genannt). Dann folgt ein Reaktionspfeil () bzw. bei einer Gleichgewichtsreaktion ein Doppelpfeil (), und auf der rechten Seite stehen die Produkte. Gegebenenfall wird gesondert auch die Reaktionsenthalpie angegeben. Für die Knallgasreaktion, bei der gasförmiger Wasserstoff mit gasförmigem Sauerstoff explosionsartig zu liquidem (=flüssigen) Wasser reagiert, ergibt sich beispielsweise unter Berücksichtigung der Aggregatzustände folgende Schreibweise:
Reaktionsschema
Der prinzipielle Ablauf einer chemischen Reaktion kann auch durch ein Reaktionsschema veranschaulicht werden, bei dem die stöchiometrischen Verhältnisse unberücksichtigt bleiben. Das kann z.B. in Form einer allgemein verständlichen Wortgleichung geschehen, z.B. für die Knallgasreaktion:
In der organischen Chemie werden im Reaktionsschema zumeist nur die Strukturformeln der beteiligten organischen Verbindungen angeschrieben. So ergibt sich etwa für die säurekatalysierte Abspaltung von Wasser aus 2-Pentanol folgendes Schema:

Als Nebenprodukt entsteht 1-Penten (links direkt nach dem Reaktionspfeil) und als Hauptprodukte die beiden Isomere (E)-2-Penten (Mitte) und (Z)-2-Penten (rechts); die Säurekatalyse und das abgepaltene Wasser werden als bekannt vorausgesetzt und nicht angeschrieben.
Beispiele
Eine einfache chemische Reaktion ist die Verbrennung, bei der ein brennbarer Stoff mit dem Sauerstoff (lat. Oxygenium; abgeleitet von griech. ὀξύς oxys „scharf, spitz, sauer“ und γεν- gen- „erzeugen“) der Luft unter Energieabgabe reagiert. So entsteht etwa bei der Verbrennung von Kohlenstoff mit einer ausreichenden Menge Sauerstoff das gasförmige Kohlendioxid (bzw. bei Sauerstoffmangel das sehr giftige Kohlenmonoxid):
Eine anderes Beispiel ist die rechts im Bild gezeigte stark exotherme Thermitreaktion von Eisen(III)-oxid und Aluminium, bei der Temperaturen bis über 2000 °C erreicht werden:
Das Bild rechts ganz oben zeigt die Reaktion von metallischem Natrium mit Wasser. Das bei der Reaktion gebildete Wasserstoffgas entzündet sich, verbrennt explosionsartig und reißt geschmolzene Natriumtröpfchen mit, die zu Natriumoxid bzw. Natriumperoxid verbrennen:
Friedrich Wöhlers Harnstoffsynthese (1828)
Als es dem deutschen Chemiker Friedrich Wöhler (1800-1882) erstmals 1828 gelang, Harnstoff aus der salzartigen anorganischen Verbindung Ammoniumcyanat herzustellen, galt dies als Beweis, dass die Synthese organischer Verbindungen keiner besonderen „Lebenskraft“ bedürfe:
Wöhler erkannte dabei ganz richtig, dass die intermediär gebildete Verbindung Ammoniumcyanat (NH4NCO) die eigentliche Harnstoffquelle darstellte:
Biochemische Reaktionen
Biochemische Prozesse, die für den Stoffwechsel aller Lebewesen von zentraler Bedeutung sind, laufen stets nur in Anwesenheit eines meist sehr komplex gebauten Katalysators in nennenswerter Geschwindigkeit ab. So katalysiert etwa das Enzym Triosephosphatisomerase (TIM, TPI) in einem Teilschritt der Glycolyse, dem lebenswichtigen Zuckerabbau in allen Organismen, die Umwandlung von Dihydroxyacetonphosphat (DHAP) zu Glycerinaldehyd-3-phosphat (GAP):
Photochemische Reaktion
Photochemische Reaktionen werden nicht primär durch Wärme, sondern durch Lichtenergie bewirkt bzw. ausgelöst. Ein komplexes Beispiel dafür ist die Photosynthese.
Siehe auch
- Kategorie:Chemische Reaktion - Artikel in der deutschen Wikipedia
- Chemische Reaktion - Artikel in der deutschen Wikipedia
- Aktivierungsenergie - Artikel in der deutschen Wikipedia
- Reaktionsenthalpie - Artikel in der deutschen Wikipedia
Einzelnachweise
- ↑ Otto Sackur, Cl. v. Simson: Lehrbuch der Thermochemie und Thermodynamik, Verlag von Julius Springer, Berlin 1928, S. 94f. google
- ↑ A. F. Holleman, E. Wiberg: Lehrbuch der Anorganischen Chemie. 71.–80. Auflage. de Gruyter, Berlin 1971, S. 57–58.
- ↑ Eintrag zu stoichiometric number. In: IUPAC Compendium of Chemical Terminology (the “Gold Book”). doi:10.1351/goldbook.S06025 Version: 2.3.1.
- ↑ Schülerduden Chemie, Bibliografisches Institut & F.A. Brockhaus AG, Mannheim 2007, ISBN 978-3-411-05386-5, S. 195.